颅咽管瘤
概述:颅咽管瘤(craniopharyngioma)起源于垂体胚胎发生过程中残存的扁平上皮细胞,是一种常见的先天性颅内良性肿瘤,大多位于蝶鞍之上,少数在鞍内。颅咽管瘤的异名很多,与起始部位和生长有关,如鞍上囊肿、颅颊囊肿瘤、垂体管肿瘤、造釉细胞瘤、上皮囊肿、釉质瘤等。
颅咽管瘤起病多在儿童及青少年。其主要临床特点有下丘脑-垂体功能紊乱、
颅内压增高、视力及视野障碍、
尿崩症以及神经和精神症状。CT扫描可明确诊断。治疗主要为手术切除肿瘤。
19世纪末,一些病理学家注意到一类罕见的生长于蝶鞍区的上皮肿瘤,认为该类肿瘤可能起源于垂体管或颅颊囊。1904年Erdheim详细描述了肿瘤的组织学特征,并认为肿瘤可能来自退化不全的垂体――咽管的胚胎扁平上皮细胞。以后人们发现颅咽管瘤的生长正是沿着颅颊囊的发生路径从咽部长到鞍底、鞍内、鞍上及第三脑室前端。有人注意到成人和儿童颅咽管瘤之间的差异,认为成人的肿瘤不是胚胎源性的,而是生后产生于垂体细胞的组织转化,因为垂体中存在扁平上皮细胞,但这一解释仍缺少证据。1910年Lewis首先尝试切除该类肿瘤。1918年后颅咽管瘤这一名称开始普遍化使用。
 流行病学
流行病学
流行病学:颅咽管瘤为常见鞍区肿瘤。在成人中颅咽管瘤的发病率仅次于垂体瘤;占儿童鞍区肿瘤的首位。颅咽管瘤的流行病学研究Bumin GR报道,1990~1993年美国中央脑肿瘤注册部统计135例。肿瘤发生率为0.13/(10万・年)。美国每年能有338例,96%发生于0~14岁儿童。无种族差异。在成人,颅咽管瘤约占
颅内肿瘤总数的4%~6%,占先天性
颅内肿瘤的60%,占垂体部肿瘤的30%,占儿童
颅内肿瘤的9%~13%,也是儿童最常见的先天性肿瘤。
颅咽管瘤在任何年龄均可发病,最大年龄的手术患者为71岁,但好发于5~15岁的儿童。总结较多报道组,发病高峰年龄在7~13岁,20~25岁,60~65岁。男女发病率的报道不一,多数报道男性多于女性,约为1.4~2.1。
 病因
病因
病因:本病为先天性疾病,生长缓慢。正常胚胎发育时,Rathke囊与原始口腔相连接的细长管道即颅咽管,此管随胚胎发育而逐渐消失。Rathke囊前壁的残余部分,前叶结节部,退化的颅咽管的残存鳞状上皮细胞都可能成为发生颅咽管瘤的起源。因此颅咽管瘤可发生于咽部、蝶窦、鞍内、鞍上及第三脑室,有的可侵入颅后窝。
大多数颅咽管瘤起源于颅颊管靠近漏斗部的残余鳞状上皮细胞,故肿瘤位于鞍上,形成所谓“鞍上型”颅咽管瘤;少数肿瘤起源于中间部的残余细胞,则肿瘤位于鞍内,形成所谓“鞍内型”颅咽管瘤。部分颅咽管瘤在鞍上和鞍内都有,则肿瘤呈哑铃形。
 发病机制
发病机制
发病机制:
1.发病机制 有关颅咽管瘤的组织发生,目前有两种学说比较普遍被人们接受。
(1)先天性剩余学说:这是被人们比较广泛接受的组织发生学说。Erdheim最早观察到正常垂体的结节部有残存的鳞状上皮细胞,认为颅咽管瘤起源于这些残余的上皮细胞。在胚胎时期的第2周,原始的口腔顶向上突起形成一个深的盲袋,称为Rathke袋,随着进一步发育,Rathke袋的下方变窄而呈细管状,即称之为颅咽管或垂体管。在正常情况下,胚胎7~8周颅咽管即逐渐消失,在发育过程中常有上皮细胞小巢遗留,即成为颅咽管瘤的组织来源。
(2)鳞状上皮化生学说:1955年Luse和Kernohan观察了1364例尸检的垂体腺,结果发现仅24%有鳞状上皮细胞巢,其出现率随年龄的增长而增高,20岁以下者鳞状上皮细胞巢出现率很低,因此,他们认为鳞状上皮细胞巢是垂体细胞化生的产物,而不是胚胎残留。另外,还有人观察到垂体腺细胞和鳞状上皮细胞的混合,并且见到二者之间有过度,这一发现也支持化生学说。
2.病理改变 颅咽管瘤体积一般较大,肿瘤形态常呈球形、不规则形,或结节状扩张生长,无明显包膜,界限清楚,范围大小差异明显,大多为囊性多房状或部分囊性,少数为实质性,只含少数小囊腔。瘤体灰红色,囊液可为黄色、棕色、褐色或无色。如囊肿破裂,囊液溢出,可引起
脑膜炎和蛛网膜炎。囊性者多位于鞍上,囊性部分常处于实质部的上方,囊壁表面光滑,厚薄不等,薄者可如半透明状,上有多处灰白色或黄褐色钙化点或钙化斑,并可骨化呈蛋壳样,囊内容为退变液化的上皮细胞碎屑(角蛋白样物),囊液呈机油状或金黄色液体,内含闪烁漂浮的胆固醇结晶,一般10~30ml,多者可达100ml以上。肿瘤实质部常位于后下方,呈结节状,内含钙化灶,有时致密坚硬,常与颅内重要血管、垂体柄、视路及第三脑室前部等粘连较紧并压迫上述结构。肿瘤亦可引起脑组织的胶质反应带形成假包膜,有时可呈乳头状突入丘脑下部,手术牵拉肿瘤时可能造成
丘脑下部损伤。实质性肿瘤多位于鞍内或第三脑室内,体积较囊性者为小。
肿瘤组织形态可分为牙釉质型和鳞形乳头型两种。牙釉质型多见,主要发生于儿童。此型最外层为柱状上皮细胞,向中心逐渐移行为外层呈栅栏状,内层细胞排列疏松的星状细胞。瘤组织常有退行性变、角化及小囊肿,囊内脱落细胞吸收钙后形成很多散在钙化灶为颅咽管瘤的显著特征,几乎所有颅咽管瘤在镜下都可见到钙化灶,大多数病例在放射检查时可发现钙化灶。颅咽管瘤常伸出乳头状突起进入邻近脑组织(特别是下丘脑),使得肿瘤与这些脑组织紧密相连,故手术时常不易完全剥去。鳞形乳头型由分化良好的扁平上皮细胞组成,其中隔有丰富的纤维血管基质,细胞被膜自然裂开或由于病变裂开而形成突出的假乳头状,一般无釉质型的角化珠、钙化、炎性反应及胆固醇沉积,此型多为实体性肿瘤。偶有报道颅咽管瘤生长迅速,呈侵袭性复发,但多数学者并不认为是恶性变,一些电镜下有间变表现的肿瘤,在组织培养中虽有成囊的倾向,但几乎无有丝分裂的活性。
颅咽管瘤的血供因发生部位不同而有差异,鞍上肿瘤的血供主要来自于Willis环前循环的小动脉,也有认为有直接来自颈内动脉,后交通动脉的供血。但颅咽管瘤不接受来自大脑后动脉(或基底动脉)的供血,除非肿瘤接近该血管供血的第三脑室底部。鞍内肿瘤的血供来自海绵窦内颈内动脉的小穿透动脉。
肿瘤向四周生长可压迫视神经交叉、脑垂体、第三脑室底部、丘脑下部、甚至阻塞一侧或两侧的室间孔而引起阻塞性脑积水。鞍内型肿瘤大多为实质性,体积较小,早期限于鞍内可直接压迫垂体,以后向上生长可影响视神经、视交叉及第三脑室。
 临床表现
临床表现
临床表现:颅咽管瘤可见于任何年龄,但以6~14岁最多见。其临床表现包括以下几个方面:肿瘤占位效应及阻塞室间孔引起的高颅压表现;肿瘤压迫视交叉、视神经引起的视力障碍;肿瘤压迫下丘脑、垂体引起的下丘脑-垂体功能障碍;肿瘤侵及其他脑组织引起的神经、精神症状。
大多数颅咽管瘤呈间歇性生长,故总体上看肿瘤生长较慢,其症状发展也慢;少数颅咽管瘤生长快速,其病情进展亦较快。
颅咽管瘤的体积较大,作为颅内占位性病变,它可直接通过占位效应引起
颅内压升高。颅咽管瘤还可压迫第三脑室,阻塞室间孔而使
颅内压升高,这可能为其引起高颅压最主要的原因。高颅压最常见的表现为
头痛,可轻可重,多于清晨发生,伴有呕吐、耳鸣、
眩晕、畏光,也可有发热、颜面潮红、出汗等自主神经功能紊乱的表现。
头痛多位于眶后,也可为弥漫性并向后颈、背部放射。肿瘤压迫第三脑室,阻塞室间孔还可引起阻塞性脑积水。偶尔瘤内囊肿破裂,囊液溢出,可引起化学性
脑膜炎和蛛网膜炎,表现为突然出现的剧烈
头痛、呕吐,伴脑膜刺激症状。
肿瘤如向两侧生长,侵入颞叶,可引起
颞叶癫痫。肿瘤向下扩展,侵及脑脚,可产生痉挛性偏瘫,甚至出现去大脑强直状态。部分病人可出现精神失常,表现为记忆力减退甚至丧失、情感淡漠,严重者神志模糊或
痴呆。
肿瘤压迫视交叉可引起视野缺损,常见的为两颞侧偏盲,两侧受损程度可不一致。如肿瘤只压迫一侧视束,则产生同向偏盲。如果肿瘤严重压迫视交叉,可引起原发性
视神经萎缩;如肿瘤侵入第三脑室,引起脑积水和
颅内压增高,则可产生继发性
视神经萎缩。眼运动神经可受累,产生复视等症状。少数病人嗅神经和面神经也可受累,表现为嗅觉丧失和
面瘫。
颅咽管瘤压迫下丘脑及垂体还可引起多种内分泌代谢紊乱和下丘脑功能障碍:肿瘤破坏视上核或神经垂体,可引起
尿崩症,其发生率约20%;肿瘤侵及下丘脑口渴中枢可引起病人烦渴多饮或口渴感丧失;肿瘤侵及饱食中枢,可引起多食或厌食;肿瘤侵及体温调节中枢,可出现发热;肿瘤损及垂体门脉系统或直接侵及腺垂体可引起腺垂体功能减退,肿瘤破坏下丘脑TRH、CRH、GnRH神经元可分别引起TSH、ACTH和促性腺激素的不足;肿瘤损及下丘脑抑制性神经元,则可引起垂体功能亢进,常见的表现有性早熟、
肢端肥大症、皮肤色素加深、皮质醇增多症等;部分病人有
肥胖、嗜睡、精神失常、血管舒缩功能紊乱等症状。
腺垂体功能减退较垂体功能亢进常见,尤以LH/FSH和GH缺乏较多见。据报道,儿童患者约50%有生长延迟,约10%的患儿出现明显的矮小症伴性发育不全。成年患者GH缺乏的表现不突出,但有性功能减退的在30%以上。TSH不足引起的继发性甲状腺功能减退约见于1/4的病人,ACTH不足引起的继发性
肾上腺皮质功能减退亦不少见。
 并发症
并发症
并发症:颅咽管瘤生长缓慢,病程较长,主要损害视丘下部及周围的结构,引起内分泌功能紊乱,视力、视野损害和
颅内压增高。治疗以手术为主。常见术后并发症如下:
1.中枢性高热 患者高热持续不退,呈
昏迷状态,预后较差,通常予以对症处理。原因可能是:①颅咽管瘤切除时下丘脑功能受损,引起体温调节功能障碍而致高热;②囊性肿瘤内的囊液刺激脑膜及下丘脑产生无菌性
脑膜炎;③手术所致血性脑脊液刺激引起发热。
术后严密观察热型及持续时间,区别中枢性高热与肺部、泌尿系感染所致高热。发热患者慎用冬眠药物,以防引起
意识障碍。术后给予头枕冰袋、冰帽或全身冰毯,持续肛温监测,体温迅速控制在38.5℃以下。为手术时下丘脑损伤所致。
2.
意识障碍 主要是丘脑下部受损或
颅内压增高引起。
颅内压增高原因:①术后血块阻塞导水管致脑积水;②手术止血不彻底引起硬膜下血肿或硬膜外血肿;③手术刺激或电解质紊乱引起继发性脑水肿。护士应严密观察患者神志及瞳孔的变化,尤其术后72h内要观察患者有无恶心、呕吐及伤口张力增加、
颈强直等症状,保持引流管畅通,注意观察引流液颜色及量。对有
意识障碍者,采用Glasgow
昏迷计分法评价意识程度。及时发现、及时正确处理。
3.
尿崩症 在肿瘤全切除或根治性次全切除的病人几乎不可避免地发生该并发症,为手术时损伤垂体柄所致。垂体柄受损后,ADH的释放是三时相的。最初,垂体柄受损后ADH释放减少致
尿崩;之后神经垂体轴突末梢变性释放出超生理量的ADH,这一释放过程常见于垂体柄损伤后48~96h,如果此时给予患者长效(油剂)抗利尿制剂(通常给短效后叶加压素),就可能导致内源性的ADH释放而引起肾功能下降;当变性的神经末梢释放的激素耗竭后,将再次发生
尿崩。一般
尿崩症持续数天至2周可恢复,但亦有少数可为永久性
尿崩症。处理如下:
(1)重点观察患者多饮、多尿、烦渴等表现及尿量、尿比重,记录24h出入量,根据出入液量补充液体。尿量<5000ml/d,可不用药物。神志清醒者嘱多饮水;神志恍惚者,术后2~3h给予留置胃管,补充水分及营养。尿量>5000ml/d,尿比重<1.005,用垂体后叶素5U皮下注射,1次/d,或
尿崩停0.3ml,1次/d,肌注。
尿崩轻者通常先给氢氯噻嗪(双氢克尿塞)、卡马西平口服治疗,严重者可应用短效后叶加压素,其间要注意控制入液量,以防止水中毒(此时病人可有水肿、抽搐等症发生)。
(2)定期测血清钠、钾、氯、二氧化碳结合率,及酸碱度和血尿素氮等。术后3~5天每12小时测电解质1次。若电解质丢失,可按正常补充;若引起钠滞留(血钠升高及渗透压增高),应限制钠盐摄入;低钠低氯患者补充氯化钠以防脑水肿;为防止低血钾给予口服氯化钾,尿量1000ml补氯化钾1g。此外,须维持钾、钙、糖在正常水平。
4.循环衰竭 术前病人有明显垂体功能减退者,术后易产生急性肾上腺皮质衰竭现象,病人呈休克状态。处理是术前应予补充激素,术后有衰竭现象者给予大剂量肾上腺皮质激素。这不仅可以减少危象,也可减少下丘脑反应及脑水肿,对中枢性高热的预防亦有积极作用。但为减少诸如感染、消化道出血等并发症,应在术后4天逐渐减少用量,一般用维持量2周后逐步停止(垂体功能障碍明显者除外)。
5.癫痫 因手术创伤和下丘脑牵拉受损,在麻醉清醒后发生癫痫。术前口服苯妥因钠0.1g,3次/d;术毕肌注安定10mg或苯巴比妥0.1g以预防。术后监测脑电图或观察患者有无口角抽动、眼睑震颤、手指抽动等迹象,发现异常在抽搐前即及时用药,癫痫发作时重复用药,同时保持呼吸道通畅,给予氧气吸入,防止脑组织缺氧。
6.消化道出血 因丘脑下部受损后反射性引起胃黏膜糜烂、溃疡致
上消化道出血及大量应用皮质激素后。病人可有黑便、呕血,甚至急性胃穿孔等。
术后应用甲氰咪呱,严密观察血压、脉搏及大便颜色。留置胃管者,观察胃内食物的消化情况及胃液颜色。突发呕血、黑便、脉率快,经输血、冰盐水洗胃,胃内注入1000IU凝血酶,1次/4h,并应用奥美拉唑、甲氰咪呱等,给予输血,应用止血剂、H2受体阻断药等,并禁食、胃肠减压、停用激素等,必要时手术治疗,使出血得到及时控制。
7.无菌性
脑膜炎 系肿瘤囊内容物在术中溢出刺激脑膜所致。为此,术中应尽可能多地切除肿瘤,用生理盐水反复冲洗囊腔。术后可多次腰穿排放脑脊液,激素的应用对缓解发热等症状亦有帮助。
8.视力障碍 术中损伤视路及其供应的血管可致视力障碍,尤其是视交叉前置型的肿瘤发生率较高,应予注意。
9.垂体功能低下 尤其是术前有垂体功能减退者,一般较难恢复。患儿生长迟缓、身材矮小、性发育不全等。处理予以甲状腺激素等药物及加强锻炼,可望有某些程度的恢复,但把握不大。
10.其他 颅咽管瘤瘤囊内放射性核素内照射治疗后并发症,各家报道可综合为:损伤视神经交叉、视束、下丘脑、放射性脑组织坏死、血管栓塞,以及放疗诱发肿瘤等。极少数肿瘤复发或死亡。
 实验室检查
实验室检查
实验室检查:普通实验室检查无特殊。内分泌功能检查多数病人可出现糖耐量曲线低平或下降延迟,血T3、T4、FSH、LH、GH等各种激素下降。少数表现为腺垂体功能亢进,大多数表现为程度不等的腺垂体及相应靶腺功能减退。
1.
生长激素(GH)测定和GH兴奋试验 颅咽管瘤患儿血清GH值降低,且对
胰岛素低血糖、
精氨酸、左旋多巴等兴奋试验,无明显升高反应,占66.7%。
2.促性腺激素(GnH) 尿促性素(FSH)、
黄体生成素(LH)测定和GnH兴奋试验。颅咽管瘤患者血清FSH、LH水平降低,且对促性腺激素释放激素(常用的为LH-RH)兴奋试验无明显升高反应,提示肿瘤侵及下丘脑-垂体区。
3.泌乳素(PRL)测定 患者血清PRL水平可升高,此可能由于肿瘤阻断泌乳素释放抑制激素(PIH)进入垂体,使PRL分泌和释放增加,可致溢乳、闭经。占50%。
4.促腺上腺皮质激素ACTH、
促甲状腺激素TSH测定 当肿瘤严重压迫垂体组织而萎缩时,患者血清ACTH、TSH均降低。
5.
抗利尿激素(ADH)测定 颅咽管瘤患者血清ADH常降低。
6.腰椎穿刺 有颅内压增高者,可出现腰穿测压升高,脑脊液化验多无明显变化。
 其他辅助检查
其他辅助检查
其他辅助检查:
1.颅骨X线平片 80%~90%的病人头颅X线平片有异常改变。儿童头颅平片有异常改变的占94%,成人占60%。主要异常表现为以下三个方面。
(1)肿瘤钙化:颅咽管瘤的钙化有各种形态,为颅咽管瘤的显著特征,鞍上型和鞍内型肿瘤均有钙化,而其他鞍部病变极少出现钙化(钙化发生率多在1%以下)。钙化在儿童中比成人中常见,儿童颅咽管瘤钙化发生率70%~85%,2岁以下者占20%,2岁以上儿童钙化者占80%,15岁以上者占50%,成人约35%左右。儿童鞍内钙化时,应高度考虑为颅咽管瘤。钙化灶可大可小,可分散,也可集中在一起,有时可呈弯曲细线状。钙化常出现在中线区,偶尔较大的病变可以只限于周围部分钙化。60%~81%的病人出现肿瘤钙化斑,呈单个或散在状,亦可融合成蛋壳状。
(2)蝶鞍改变:儿童患者因TSH和GH缺乏,骨X线片可显示骨龄减小。绝大多数颅咽管瘤位于蝶鞍的上部,可向下压迫蝶鞍,故在头颅平片上可发现蝶鞍变扁平,床突受损。少数颅咽管瘤位于鞍内,在头颅平片上可见蝶鞍扩大。实际上任何类型的蝶鞍改变都可以见于颅咽管瘤,可以是典型的鞍上肿瘤改变,也可以是鞍内肿瘤的改变。35%病人蝶鞍呈盆形或球形扩大或破坏,后床突及鞍背可削尖、脱钙、消失。蝶鞍有明显的改变时,常提示有巨大的病变,反之则不一定。
(3)颅内压增高征象:60%病人在头颅X线平片上可见颅内压增高的征象,表现为鞍背脱钙,颅骨内板脑回压迹明显、颅底变平等表现,小儿可有颅骨骨缝分离等
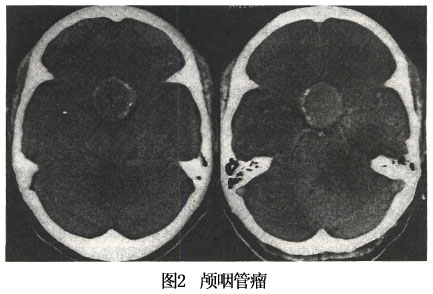
2.CT扫描 颅脑CT扫描显示为鞍区肿瘤改变,非增强扫描者实质性肿瘤表现为高密度或等密度影像,钙化斑为高密度,囊性者因瘤内含胆固醇而呈低密度像,CT值为-40~10Hu,囊壁为等密度。病变边界清楚,呈圆形、卵圆形或分叶状,两侧侧脑室司扩大。强化扫描时约2/3的病例可有不同程度的增强,CT值增加12~14Hu,囊性颅咽管瘤呈环状强化或多环状强化而中心低密度区无强化,少数颅咽管瘤不强化。一般具有钙化、囊腔及强化后增强三项表现的鞍区肿瘤,即可确诊为颅咽管瘤(图1,2)。
3.MRI 多数颅咽管瘤囊性部分所含的物质呈短T1与长T2,但也可呈长T1与长T2像,即T1加权像上呈低信号,T2加权像上呈高信号;若为实质性颅咽管瘤,则呈长T1与长T2。钙化斑呈低信号区。
CT和MRI检查对诊断具有重要意义,此2项检查可显示肿瘤的位置、大小、有无囊变、肿瘤对邻近脑组织的侵袭情况、是否有脑积水存在。一般来说,MRI在显示肿瘤的结构及其与邻近脑组织(如视交叉)的关系方面优先于CT,但他不能像CT那样显示钙化灶。
4.脑室造影 因肿瘤大小各异,脑室造影能明显显示肿瘤对颅底动脉的影响和变化,对手术极有帮助。肿瘤囊腔是否与脑室相通,可在行脑室造影的同时,可直接穿刺入肿瘤囊腔。
5.脑电图 以额部或广泛的δ波或θ波为主。
 诊断
诊断
诊断:任何年龄的病人如出现高颅压、神经眼科症状及下丘脑-垂体功能紊乱均应考虑颅咽管瘤的可能。根据好发部位、临床表现及辅助检查诊断颅咽管瘤并不困难。凡青少年儿童出现内分泌功能障碍,如发育矮小、多饮多尿、
肥胖、生殖器发育不良等,均应首先考虑本病;若有鞍上或鞍内钙化斑,更有助于诊断。若成人出现性功能障碍或
头痛、视力视野障碍,也应考虑本病。
少数临床表现不典型者、临床症状轻微者诊断不易,关键是要提高对本病的警惕性。通过实验室检查、CT和MRI对诊断具有重要的意义,对疑似病例应及时做此种检查,以免延误诊断。
 鉴别诊断
鉴别诊断
鉴别诊断:以高颅压为主要表现的颅咽管瘤需与其他颅内占位性病变鉴别;以视力、视野改变的需与其他鞍部病变如垂体腺瘤、视神经胶质瘤、鞍区
脑膜瘤、颈内动脉瘤及胚组织瘤等相鉴别,因为这些鞍部病变亦可损及视交叉、视神经及视束而引起类似症状;以腺垂体功能减退为主要表现的需与其他引起腺垂体功能减退的疾病相鉴别。
1.垂体腺瘤 颅咽管瘤应首先与垂体腺瘤相鉴别,因为两者均可出现内分泌及视力障碍,临床表现相似,有时实质性颅咽管瘤鞍内型在CT上也难以与垂体腺瘤相区别。垂体腺瘤占鞍区肿瘤的第一位,多见于20~50岁成人,以视力、视野障碍为主要表现,多为双颞侧偏盲,眼底几乎均为原发性视神经乳头萎缩。垂体前叶功能低下为主,而无生长发育迟缓,一般不产生
颅内压增高。蝶鞍多呈球形扩大而无钙化。CT扫描表现为等密度或略高密度肿块,强化扫描可见均匀增强。
2.鞍结节脑膜瘤 除了垂体腺瘤及颅咽管瘤,鞍区肿瘤即属鞍结节脑膜瘤常见,居第三位。25~50岁为高发年龄。早期一般无内分泌障碍,可有视力障碍及
头痛。晚期可出现视野障碍及眼底原发性视神经乳头萎缩。蝶鞍改变不明显,有的可见鞍结节增生或破坏,钙化少见。CT扫描呈略高或等密度肿块,肿瘤呈均匀明显强化。
3.鞍区生殖细胞瘤 即异位松果体瘤,占第四位,70%病人年龄分布在7~20岁。多有内分泌障碍,但以
尿崩症为突出症状,可伴有性早熟,亦可有视力、视野改变。蝶鞍正常。
4.视交叉胶质瘤 多发生在7~20岁,内分泌症状少见,多以视力改变为主,表现为单眼突出、视力障碍、
头痛等。视神经孔多扩大,无钙化。CT扫描为低密度肿块,一般无强化或轻度强化。
5.鞍区表皮样囊肿 很少见,绝大多数发病年龄在23~37岁之间,以视力、视野障碍为主要表现,一般无内分泌障碍,
颅内压增高症状也很少发生。蝶鞍正常、无钙化,CT扫描示鞍区低密度病灶,CT值多为负值,不强化。
6.脊索瘤 多发生在35岁左右,以多条脑神经损伤为主要表现,常有钙化,蝶鞍部及斜坡部有明显骨质破坏。CT显示为不规则略高密度肿块,其中有钙化点,多数不发生强化,少数可有均匀轻度强化。
7.鞍区动脉瘤 罕见,多见于中年人,以突然发病、
头痛、动眼神经
麻痹为特征,蝶鞍一般无改变,脑血管造影可确诊。术中穿刺为鲜血,肿物不塌陷。
8.第三脑室前部胶质瘤 多发生在成年人,一般无内分泌症状,以
颅内压增高为主要表现。蝶鞍一般无改变,肿瘤很少有钙化,CT扫描可以鉴别。
9.视交叉蛛网膜炎 多见于成人,以视力、视野改变为主要表现,视野改变一般无规律,呈不规则变化,视野缩小,一般无内分泌障碍及
颅内压增高。蝶鞍正常,CT扫描无鞍区占位性病变。
10.原发性空蝶鞍 很少见,中年发病,以视力、视野障碍、
头痛为主要表现,有时出现内分泌症状,临床上有时很难与颅咽管瘤相鉴别,CT扫描显示鞍内为空腔。
11.鞍区蛛
网膜囊肿 罕见,以小儿多见,亦可见于成人,主要症状为脑积水引起的颅内高压,可有视力、视野改变,少数病人有内分泌症状,蝶鞍扩大或双鞍底,CT扫描见脑脊液密度的圆形低密度区。
颅咽管瘤与上述诸疾病的鉴别主要依靠以下2点:上述诸疾病除引起与颅咽管瘤类似的表现外,还有其他不符合颅咽管瘤的表现;上述诸疾病和颅咽管瘤在影像学上表现不同。一般来说,通过CT和MRI检查,结合临床表现,绝大多数病例可得明确诊断。极少数病例可能需要依赖手术标本的病理检查始能确诊。
 治疗
治疗
治疗:外科手术为颅咽管瘤的首选治疗方法。对于实质性肿瘤,手术可切除瘤体;对于囊性肿瘤,手术可放去囊液,从而缓解肿瘤的压迫症状。小的颅咽管瘤特别是鞍内型肿瘤一般采取经蝶术式,大瘤宜采取经颅术式。一般来说,成功的手术可有效缓解视交叉受压引起的视力、视野改变以及高颅压引起的头痛等症状,还能使腺垂体功能得到恢复。不过,很多鞍上型颅咽管瘤与周围脑组织(特别是下丘脑)紧密相连,增加了手术的难度,对这些病人并不强求完全切除肿瘤,可采取部分切除,部分切除的缺点是术后复发率很高。手术的死亡率约10%,术后5年复发率为25%~75%。腺垂体功能减退为手术治疗的主要副作用,其发生率达75%。
早在1937年,有人就采用放射线治疗颅咽管瘤。一般采用外照射的方法。由于大多数颅咽管瘤用手术方法不能完全切除,而其化疗又不敏感,故主张术后加用放射治疗。颅咽管瘤的术后复发率高,而再次手术的风险很大,故对复发病人也只能采用放射治疗。近年,有人采用立体定向技术植入胶体磷(32P)酸铬、胶体钇(90Y)、胶体金(198Au)治疗颅咽管瘤,也取得了成功,其优点为放射损伤小。
放射治疗的副作用主要有:放射性视神经炎、蝶鞍及鞍周脑组织的放射性坏死、垂体功能减退等。这些副作用的发生率随剂量的增加而增加,如剂量超过60Gy,视神经炎的发生率可达30%,脑坏死的发生率也达12.5%。放射治疗引起的腺垂体功能减退主要表现为GH和LH/FSH的缺乏。据报道,GH缺乏的发生率几近100%,且出现很快(于照射3天后即可出现),数月后病儿的生长即受影响。LH/FSH缺乏的发生率亦很高,但出现较GH缺乏为迟,表现为性发育障碍(儿童)或性功能不全(成人)。GH缺乏的原因可能为下丘脑受损,因为用GHRH治疗有效。目前认为,LH/FSH缺乏的部位也在下丘脑。值得注意的是,部分病人于放射治疗后反而出现性早熟,其机制未明。
对高颅压者应立即给予脱水剂和利尿剂,以降低颅内压,此类患者应尽快做术前准备,行手术治疗。术前有腺垂体功能减退者,应注意补给足量的糖皮质激素,以免出现垂体危象。对其他腺垂体激素可暂不补给,因不少病人于术后腺垂体功能可得到恢复;如术后仍有腺垂体功能减退,应给予相应的治疗。手术或放射治疗引起的腺垂体功能减退一般为永久性,应予治疗。
 预后
预后
预后:
1.手术效果与预后 过去该瘤的手术全切除率低,致死致残率及复发率高。近30余年来开展显微手术,对保护正常脑组织、争取肿瘤全切除、减少下丘脑及垂体损伤,降低致残率及死亡率创造了有利条件,大大地改善了病人的预后。有人报道颅咽管瘤的手术死亡率已降至2%,10年生存率达58%~66%,复发率为7%~26.5%。国内同济医科大学、解放军总院等单位进行的肿瘤全切除或积极手术切除,手术死亡率为4%~6%,肿瘤复发10%,取得较好疗效。
2.放疗效果与预后 由放疗引起的神经后遗症很少。从神经、智力、精神以及内分泌功能来评价颅咽管瘤放疗长期效果在功能方面的变化不比手术治疗差。全切除与次全切除后辅以放疗的病人,两组结果相似。Richmond报告颅咽管瘤放疗后10年以上的生存率达44%~100%;Manaka对125例颅咽管瘤病人进行放疗效果评价,结果5年及10年生存率分别为88.9%和7.6%,对照两组仅分别为34.9%和27.1%,平均生存时间放疗组大于10年,而对照组为3.12年。Kramer报道6例15岁以下儿童经放疗后20年无症状,且无脑坏死现象;Pollack报告的放疗病例,经14~45个月随访,所有病例症状均有改善,肿瘤囊壁明显缩小。
3.瘤内/瘤腔内化疗效果与预后 Takahashi报告7例采用瘤内注射博来霉素治疗颅咽管瘤,4例囊性者,平均随访5年,经CT扫描均无复发;3例实质性者,1例术后1.5个月死亡,2例暂时有好转,后因复发死亡。由于这一疗法开展不够,其治疗效果尚不能肯定。
颅咽管瘤于术后及放射治疗后发生GH缺乏的比率很高,但有相当一部分病人仍能维持几近正常的生长,并不出现矮小症,这称为没有生长激素的生长综合征(growth without growth hormone syndrome),其机制尚未阐明,有人认为与血胰岛素及其他肽类生因子水平升高有关。
 预防
预防
预防:
1.对高颅压者应立即给予
脱水剂和利尿剂,以降低颅内压,此类患者应尽快做术前准备,行手术治疗。
2.术前有腺垂体功能减退者,应注意补给足量的糖皮质激素,以免出现垂体危象。对其他腺垂体激素可暂不补给,因不少病人于术后腺垂体功能可得到恢复;如术后仍有腺垂体功能减退,应给予相应的治疗。



 流行病学
流行病学
 病因
病因
 发病机制
发病机制
 临床表现
临床表现
 并发症
并发症
 实验室检查
实验室检查
 其他辅助检查
其他辅助检查

 诊断
诊断
 鉴别诊断
鉴别诊断
 治疗
治疗
 预后
预后
 预防
预防